CENNI STORICI
La Cannabis sativa ha una lunga storia come analgesico.
W.B.O'Shaughnessey, il medico che reintrodusse nella terapia "occidentale" l'uso della Cannabis, scrisse nel 1839 di aver scoperto in essa un efficace analgesico [1]. Successivamente essa fu utilizzata in svariate condizioni dolorose, come nel dolore da parto, negli spasmi dolorosi, nelle nevralgie e nell'emicrania. Ancora nel 1962 Benigni, nel suo trattato sulle erbe medicinali, scriveva:
"I suoi impieghi terapeutici sono in relazione soprattutto con l'azione analgesica di questa droga, azione molto simile a quella dell'oppio di cui la Cannabis indiana può essere considerata un succedaneo [2].
RICERCHE RECENTI
Le proprietà antidolorifiche dei cannabinoidi sono state dimostrate in vari modelli animali, usando stimoli termici [3], chimici [4], meccanici [5], e viscerali [6]. Tali composti hanno un'azione diretta su recettori del midollo spinale che mediano l'analgesia [7].
Il maggiore principio attivo della cannabis, il tetraidrocannabinolo (THC), stimola il rilascio di oppioidi endogeni, le cosiddette endorfine [8], e inibisce gli enzimi che degradano questi oppiodi [7]; i cannabinoidi posseggono inoltre effetti anestetici locali [9].
Il nostro organismo è sottoposto continuamente a stimoli potenzialmente dolorosi; a controbilanciarli possiede un sistema antidolore attivo tonicamente che però nei soggetti con dolore cronico risulta spesso meno attivo. Il sistema dei recettori cannabinoidi è attivo tonicamente e la sua attività aumenta in risposta a stimoli nocivi. Gli endocannabinoidi modulano la soglia basale del dolore, e la ridotta attività del sistema cannabinoide provoca di converso una maggior risposta agli stimoli dolorosi, la cosiddetta iperalgesia [10-12]. E' dimostrato che il cannabinoide endogeno anandamide svolge un ruolo centrale nella soppressione del dolore [13-14].
I recettori dei cannabinoidi sono distribuiti nel Sistema Nervoso Centrale(SNC) in numerose aree deputate al controllo del dolore [15]. I cannabinoidi sono inoltre in grado di stimolare altri recettori, situati al di fuori del SNC, che partecipano anche essi al controllo del dolore [16-17].
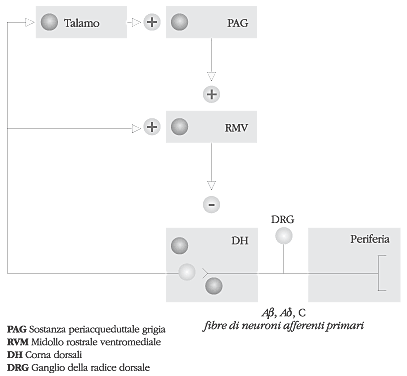
Cannabinoidi: principali siti di azione
tratta da: I cannabinoidi nel dolore [15]
Il potere antidolorifico dei cannabinoidi è blando se paragonato a quello degli oppiacei (morfina e simili): 20 mg di THC equivalgono a 120 mg di un oppiaceo "minore" quale la codeina [18].
Il meccanismo con cui i cannabinoidi producono analgesia è farmacologicamente simile, ma tuttavia indipendente rispetto a quello degli oppiacei [13].
Cannabinoidi e oppioidi hanna pertanto una azione sinergica: la somministrazione contemporanea provoca un effetto analgesico superiore a quello indotto dalla somministrazione delle singole sostanze. In virtù di ciò il THC risulta in grado di ridurre la dose minima efficace della morfina (-55%), del metadone (-75%) e della codeina (-96%) [19].
Nel luglio 2001 è uscita una rassegna sul British Medical Journal riguardante gli effetti analgesici dei cannabinoidi [20].
Lo studio, sostanzialmente negativo, è stato ampiamente ripreso dalla stampa. In realtà l'analisi prende in considerazione una casistica disomogenea e del tutto insufficiente per poter formulare considerazioni conclusive [21 -22].
Le patologie dolorose in cui la Cannabis sembra avere un ruolo degno di essere indagato in maniera approfondita sono varie.
Vi è un potenziale ruolo dei cannabinoidi per il trattamento del dolore neuropatico, area in cui attualmente pochi farmaci sono efficaci, compresa la morfina.
Nella terapia del dolore tumorale oltre l'effetto antalgico vi può essere un effetto positivo sull'appetito, con riduzione della nausea da chemioterapia; benefica l'azione sull'umore.
Un interessante campo di applicazione potrebbe ancora essere quello del dolore muscolo-scheletrico.
La Cannabis potrebbe infine avere un ruolo nel trattamento dell' emicrania, altra patologia nella quale i farmaci convenzionali risultano scarsamente efficaci o gravati da severi effetti collaterali [23].
|
|
Cos'è il dolore? |
Il dolore è un concetto intuitivo, e tutti presumiamo di sapere cos'è.
In realtà sulla definizione di dolore hanno dibattuto generazioni di scienziati, psicologi, filosofi e teologi.
Il concetto di dolore è estremamente relativo, e varia in dipendenza dalla popolazione, dal sesso e dall'individuo, e negli individui varia a seconda dei vari tipi di esperienza dolorosa.
La soglia del dolore è simile in tutti gli individui, cioè se lo stimolo è abbastanza intenso tutti i soggetti proveranno dolore; varia molto invece da individuo a individuo la soglia di tolleranza oltre a cui il soggetto non può più sopportare lo stimolo.
Data la relatività dell'esperienza dolorosa, non esiste un "termometro" del dolore. Il metodo più diffuso per valutare la sua intensità è quello di chiedere al singolo paziente quanto forte è il suo dolore in quel momento. Si ricorre di solito a un semplice strumento, chiamato Scala Analogica Visiva o V.A.S., costituito da un righello di dieci centimetri. Il punto corrispondente allo zero corrisponde a "nessun dolore", il dieci corrisponde al "massimo dolore che si può immaginare". Il paziente deve porre un cursore lungo il righello in corrispondenza del punto che equivale alla sua intensità del dolore.
Possiamo distinguere un dolore somatico, acuto e ben localizzato; un dolore viscerale, meno localizzato e spesso accompagnato da sintomi quali malessere generalizzato o nausea.
In questi due tipi di dolore si ha un danno più o meno preciso che attiva i meccanismi di allarme del nostro organismo, in modo tale che la sensazione dolorosa può essere considerata appunto un campanello d'allarme che richiede una risposta comportamentale adeguata.
Diverso è il caso del dolore neuropatico, in cui ad essere primariamente leso è proprio il sistema di transduzione del dolore: ad esempio la nevralgia che si può instaurare dopo un herpes zoster, o fuoco di Sant'Antonio.
Tale dolore, spesso di tipi urente o a scossa, è accompagnato da sensazioni cutanee anormali, spesso assai sgradevoli. Vi è inoltre risposta esagerata agli stimoli, sia dolorifici che normali. E' uno dei tipici dolori slegati da qualsiasi finalità, così come il dolore da cancro. Non si tratta più in questi casi di dolore sintomo: il dolore diventa malattia di per sé, in grado di interferire gravemente sulla vita del malato.
Per il cancro si è coniato il termine di dolore totale: al sintomo fisico si associano gli effetti collaterali delle terapie, la nausea, il vomito , la perdita di capacità fisiche, l'incertezza per il futuro, l'irritabilità, la paura della morte.
Terapie convenzionali
A parte le varie terapie fisiche o causali, l'OMS consiglia un approccio basato su una scala a tre gradini.
Il primo corrisponde all'uso dei farmaci antiinfiammatori non steroidei o F.A.N.S., cioè Aspirina e derivati.
Nel secondo si associano gli oppioidi deboli, cioè codeina e simili.
Al terzo livello corrisponde la morfina e gli altri oppioidi forti.
Naturalmente sono tutti farmaci con possibili effetti collaterali, talora gravi. I F.A.N.S. possono dare disturbi allo stomaco fino all'ulcera, specie se assunti per lunghi periodi come nel caso di dolori cronici. Gli oppioidi danno quasi sempre stitichezza anche grave, spesso nausea, torpore ed è sempre possibile, anche se rara, la depressione respiratoria. |
|